【NOW健康 連慧婷/台北報導】為因應COVID-19當前流行變異株防疫之需求,食藥署13日召開專家會議,核准莫德納XBB.1.5疫苗專案輸入。疾管署發言人曾淑慧表示,因已收到測試標準品,疫苗到貨後最快7天可以完成檢驗封緘,9月底前有望開打。
食藥署表示,經審查莫德納XBB.1.5疫苗所附資料證據,莫德納XBB.1.5疫苗與先前已核准的莫德納疫苗採用相同的技術平台製造,具有相似的特性。動物試驗及小規模免疫原性試驗結果顯示,施打莫德納XBB.1.5疫苗,可誘發對抗XBB變異株病毒(如XBB.1.5、XBB.1.16)較佳的中和抗體免疫反應,而對於重點變異株EG.5和新出現的變異株BA.2.86,亦可誘發相似的中和抗體免疫反應,可對目前流行的變異病毒株提供保護效益優勢。
在安全性方面,施打莫德納XBB.1.5 疫苗追加劑發生的局部/全身性不良反應與先前已核准的莫德納疫苗相似,以輕中度不良反應為主。
此外,食藥署也表示,考量國內目前流行的變異株以XBB變異株病毒為主,世界衛生組織亦建議使用單價XBB.1衍生譜系(如XBB.1.5)作為新疫苗抗原成分,經專家會議整體評估其臨床風險效益,同意核准莫德納XBB.1.5疫苗專案輸入,適用於6個月以上兒童、青少年及成人的主動免疫接種。未來食藥署將持續監控國內外接種COVID-19疫苗的安全警訊,分析評估疫苗不良事件通報資料,執行安全監視機制,保障民眾接種疫苗之安全。
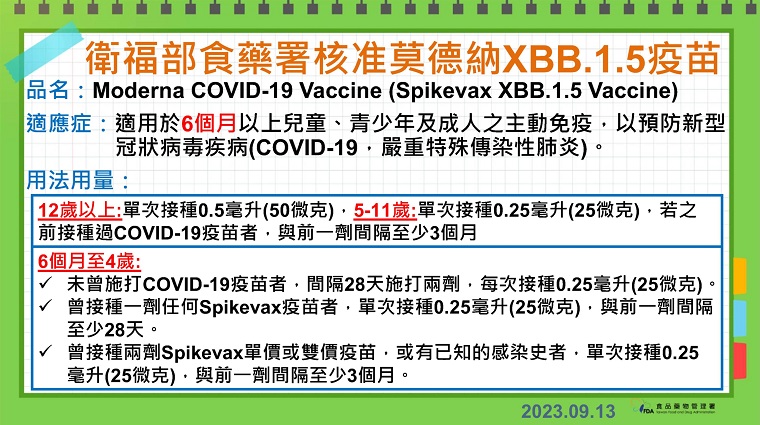
▲莫德納XBB.1.5疫苗適應症、用法與用量等相關資訊如上。(圖/食藥署提供)
曾淑慧提到,今年預計公費採購600萬劑XBB疫苗,第1批則預計採購200萬劑,會先由65歲以上民眾先開打,後續依據接種情況開放更多年齡層接種,希望讓民眾都能接種到疫苗,且若打氣不太好,也可能3天就開放擴大接種年齡層。
核稿編輯:陳珍妮
更多NOW健康報導
▸年輕人這些生活習慣埋乾眼症禍根 眼科專用脈衝光有解
▸健保署編列3億推「居家遠距醫療」 最快明年第1季上路